Холестерин — элемент, необходимый для нормальной работы организма. В то же время это одна из основных причин развития сердечно-сосудистых патологий. Так как
Что такое синдром Жильбера и как его лечить? Диагностика и причины развития. Чем опасен синдром Жильбера? Ответы на частые вопросы о заболевании от врачей АО Медицина (клиника академика Ройтберга).
Простые советы по изменению питания: растительные волокна, омега-3 жирные кислоты, орехи, авокадо, оливковое масло и др.
Почему появляется сильная потливость после коронавируса. Что делать, если странный запах тела. Как убрать сильное потоотделение после ковида.
Диета и холестерин: продукты, которые помогут улучшить ваши показатели
Может ли миска овсяной каши снизить ваш холестерин? А как насчёт горстки грецких орехов или авокадо? Несколько простых изменений в вашем питании, — и это (вместе с физической активностью и другими полезными для сердца привычками) поможет Вам снизить уровень холестерина.
Овсяная крупа, овсяные отруби и продукты, богатые клетчаткой
Овсянка содержит растворимые волокна, которые снижают уровень липопротеинов низкой плотности (ЛПНП) – так называемого “плохого” холестерина. Растворимые волокна также содержатся в фасоли, яблоках, грушах, ячмене и черносливе.
Растворимые волокна могут понизить поступление холестерина в кровь. 5-10 г и более растворимых волокон в день снижают уровень общего холестерина и ЛПНП. В полутора чашках овсяной каши содержится 6 г волокон. Если вы добавите в кашу какой-нибудь фрукт, например, банан, вы получите еще около 4 г волокон. Для разнообразия попробуйте необработанную овсяную крупу или овсяные хлопья, содержащие овсяную крупу или овсяные отруби.
Рыба и омега-3 жирные кислоты

Рыба и омега 3 жирные кислоты
Употребление жирной рыбы полезно для сердца, поскольку она содержит большое количество омега-3 жирных кислот, которые снижают артериальное давление и риск образования тромбов. У людей, перенесших инфаркты, рыбий жир и омега-3 жирные кислоты понижают риск внезапной смерти.
Кардиологи рекомендуют съедать как минимум 2 порции рыбы в неделю. Наибольшее количество омега-3 жирных кислот содержат:
Чтобы обойтись без добавления вредных жиров, рыбу следует запекать или готовить на гриле. Если вы не любите рыбу, вы можете получить некоторое количество омега-3 жирных кислот из таких продуктов, как льняная мука, рыжиковое или рапсовое масло.
Ещё один путь – это принимать пищевые добавки с омега-3 жирными кислотами или рыбьим жиром, но тогда вы не получите другие полезные вещества, которые также содержатся в рыбе (например, селен). Если вы планируете использовать такие добавки, предварительно проконсультируйтесь со своим лечащим врачом.
Грецкие орехи, миндаль и другие орехи

Польза орехов
Грецкие орехи, миндаль и другие орехи могут улучшить показатели холестерина. Богатые моно- и полиненасыщенными жирными кислотами, грецкие орехи также помогают поддерживать здоровье сосудов.
Ежедневное употребление горстки практически любого вида орехов (миндаль, фундук, арахис, пекан, кедровые орешки, фисташки, грецкие орехи) может снизить риск сердечно-сосудистых заболеваний. Выбирая орехи, следите, чтобы они были без добавления соли или сахара.
Все орехи высококалорийны, поэтому горстки (40-45 г) будет вполне достаточно. Чтобы избежать переедания и не набирать вес, замените продукты, богатые насыщенными жирами, на орехи. Например, вместо сыра, мяса или сухариков положите в салат горстку грецких орехов или миндаля.
Авокадо
Авокадо – богатый источник питательных веществ, а также мононенасыщенных жирных кислот (МНЖК). По данным последних исследований, ежедневное включение авокадо в диету улучшает показатели ЛПНП у людей, страдающих избыточной массой тела или ожирением.
Дольки авокадо можно добавлять в салаты или делать сэндвичи с авокадо. Также авокадо можно есть в качестве гарнира.
Оливковое масло

Польза оливкового масла
Чтобы получить пользу для своего сердца, старайтесь ежедневно употреблять 2 столовые ложки (23 г) оливкового масла, заменяя им другие жиры. Вы можете пассеровать овощи в оливковом масле, добавлять его в маринады или смешивать с уксусом для заправки салатов. Обжаривая мясо, пользуйтесь оливковым маслом вместо сливочного.
И авокадо, и оливковое масло – высококалорийные продукты, поэтому не ешьте их больше рекомендованного количества.
Продукты с добавлением растительных стеролов и станолов
Доступны продукты, обогащенные стеролами или станолами – растительными веществами, которые блокируют всасывание холестерина.
Некоторые маргарины, апельсиновый сок и питьевые йогурты с добавлением растительных стеролов могут снизить уровень ЛПНП на 5-15%. Для того, чтобы увидеть результаты, необходимо употреблять как минимум 2 г растительных стеролов в день, что соответствует примерно 2-м стаканам апельсинового сока, обогащенного стеролами.
Неясно, снижают ли продукты, содержащие растительные стеролы и станолы, риск инфарктов и инсультов, хотя эксперты полагают, что продукты, снижающие холестерин, также уменьшают и риск сердечно-сосудистых осложнений. Растительные стеролы и станолы не влияют на уровень триглицеридов и липопротеинов высокой плотности (ЛПВП) – так называемого “хорошего” холестерина.
Сывороточный протеин
Сывороточный протеин, один из 2-х белков, содержащихся в молочных продуктах (второй – это казеин), может объяснять многие полезные свойства молочных продуктов. Исследования показали, что сывороточный протеин в виде пищевой добавки снижает уровень как ЛПНП, так и общего холестерина.
Вы можете найти сывороточный протеин в виде порошка в магазинах здорового питания и в некоторых супермаркетах. Следуйте инструкциям по применению, указанным на упаковке.
Другие изменения в питании
Чтобы названные продукты действительно приносили пользу, вам придётся пересмотреть своё питание и скорректировать образ жизни.
Хотя выше говорилось о пользе некоторых видов жиров, употребление других — насыщенных жиров и трансжиров необходимо ограничить. Насыщенные жиры, содержащиеся в мясе, сливочном масле, сыре и других жирных молочных продуктах, а также в некоторых растительных маслах, повышают уровень общего холестерина. Трансжиры, часто используемые в маргаринах или покупном печенье, крекерах или тортах, особенно вредны для здоровья. Они повышают ЛПНП и понижают ЛПВП – т.н. “хороший” холестерин. Если на этикетке в составе продукта указаны “частично гидрогенизированные масла”, этот продукт содержит трансжиры, и лучше его избегать.
К изменению диеты следует добавить и коррекцию образа жизни в целом, – это ключ к улучшению показателей холестерина. Физические упражнения, отказ от курения и поддержание здорового веса помогут вам нормализовать уровень холестерина.
Оставьте телефон –
и мы Вам перезвоним
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Интерпретация биохимического анализа крови при патологии печени. Часть 2. Синдром холестаза
М. Г. Ипатова 1,2 к.м.н., Ю. Г. Мухина 1 д.м.н., проф., П. В. Шумилов 1 , д.м.н., проф.
1 ФГБОУ ВО РНИМУ им. Н. И. Пирогова Минздрава России, г. Москва
2 Детская городская клиническая больница № 13 им. Н. Ф. Филатова, Москва
Ключевые слова: печень, синдром холестаза, щелочная фосфатаза, гамма-глютамилтранспептидаза, лейцинаминопептидаза, 5-нуклеотидаза, желчные кислоты, билирубин, гепатопротективные препараты
Keywords: liver, cholestatic syndrome, alkaline phosphatase, gamma-glutamyltranspeptidase, leitinaminopeptidase, 5-nucleotidase, bile acids, bilirubin, hepatoprotective drugs
В статье изложены биохимические лабораторные показатели и их клиническое значение при заболеваниях печени, протекающих с синдромом холестаза. Подробно описаны механизмы действия гепатопротективных препаратов, применяемых при холестатическом синдроме.
Cиндром холестаза – нарушение синтеза, секреции и оттока желчи. В клинической практике холестаз подразделяют на внутрипеченочный и внепеченочный. Внутрипеченочный холестаз характеризуется уменьшением тока желчи и ее поступления в двенадцатиперстную кишку при отсутствии механического повреждения и обструкции внепеченочного билиарного тракта. Внутрипеченочный холестаз обусловлен либо нарушением механизмов образования и транспорта желчи на уровне гепатоцитов, либо повреждением внутрипеченочных протоков, либо сочетанием указанных факторов. Длительно сохраняющийся холестаз приводит к развитию билиарного фиброза или цирроза печени [1, 2].
Маркерами холестаза являются щелочная фосфатаза (ЩФ), гамма-глутамилтранспептидаза (ГГТ), лейцинаминопептидаза (ЛАП) и 5-нуклеотидаза. Эти ферменты локализованы в эндотелии желчных протоков и эпителии синусоидов, поэтому при холестазе под влиянием компонентов желчи они переходят в кровь.
Содержание билирубина в крови прогрессивно увеличивается обычно в течение первых 3 недель холестаза, преимущественно за счет конъюгированной фракции.
Наиболее достоверным маркером холестаза является повышение сывороточной концентрации желчных кислот, однако их определение не относится к рутинным диагностическим тестам.
Помимо вышеперечисленных показателей, при холестатическом синдроме повышается уровень липидов: холестерина, фосфолипидов, триглицеридов, липопротеидов. Однако в терминальной стадии поражения печени уровень холестерина может снижаться.
Повышение активности трансаминаз, как правило, не столь значительно, как повышение уровня маркеров холестаза. В то же время при острой обструкции магистральных протоков активность АСТ, АЛТ может быть более 10 норм.
Для пациентов с врожденными холестатическими заболеваниями важна ранняя диагностика, так как в ряде случаев для эффективного лечения достаточно заместительной терапии препаратами урсодезоксихолевой или холевой кислоты.
Щелочная фосфатаза
Референтные значения ЩФ: для новорожденных – 90–370 Ед/л; для детей до 1 года – 80–470 Ед/л, детей 1–10 лет – 65–360 Ед/л, 10–15 лет – до 440 Ед/л, старше 15 лет – до 130 Ед/л; для беременных в третьем триместре – до 250 Ед/л.
Щелочная фосфатаза (ЩФ) катализирует отщепление фосфорной кислоты от ее органических соединений. Название ЩФ получила в связи с тем, что для нее оптимальный рН – 8,6– 10,1. Фермент расположен на клеточной мембране и принимает участие в транспорте фосфора. Двухвалентные ионы, такие как Mg2+, Co2+, Mn2+, являются активаторами фермента, Zn2+ входит в структуру активного центра. Фосфаты, бораты, оксалаты подавляют активность всех форм фермента. Период полураспада фермента составляет приблизительно 7 дней. Щелочная фосфатаза содержится практически во всех органах, но максимальная ее активность выявляется в гепатобилиарной системе, костной ткани, кишечнике, плаценте, лактирующей молочной железе. Для диагностических целей чаще всего проводят определение активности костной и печеночной изоформ щелочной фосфатазы [3–5].
Костную щелочную фосфатазу продуцируют остеобласты – крупные одноядерные клетки, лежащие на поверхности костного матрикса в местах интенсивного формирования кости. Видимо, благодаря внеклеточному расположению фермента в процессе кальцификации можно проследить прямую связь между заболеванием кости и активностью фермента в сыворотке крови [6].
Активность печеночной формы фосфатазы наиболее часто повышается вследствие повреждения или деструкции гепатоцитов (печеночно-клеточный механизм) или нарушения транспорта желчи (холестатический механизм). Печеночно-клеточный механизм повышения активности щелочной фосфатазы играет ведущую роль при вирусных и аутоиммунных гепатитах, токсических и лекарственных повреждениях печени [6].
Патологические состояния, при которых повышается ЩФ, представлены в табл. 1.
Таблица 1. Причины повышения уровня щелочной фосфатазы
| Внепеченочное повышение ЩФ | Гепатобилиарные причины повышения ЩФ |
| Болезни крови: I, II стадии болезни Ходжкина, лимфогрануломатоз, другие заболевания крови | Обструкция желчных протоков (опухоль головки ПЖ, камень в общем желчном протоке, первично-склерозирующий холангит, стриктура желчных протоков, атрезия желчных протоков) |
| Заболевания кишечника: синдром мальабсорбции, воспалительные и инфекционные заболевания кишечника | Внутрипеченочный холестаз: лекарственный гепатит (некоторые антибиотики, гормональные контрацептивы и др.), первичный билиарный цирроз, отторжение печени после трансплантации |
| Патология костной системы: переломы, остеомиелит, рахит, болезнь Педжета, остеогенная саркома, метастазы в кости | Инфекционные и неинфекционные заболевания печени (острый и хронический вирусные гепатиты, некоторые наследственные заболевания обмена веществ и др.) |
| Застойная сердечная недостаточность | Аутоиммунные гепатиты |
Учитывая широкий спектр причин, вызывающих повышение ЩФ, данный фермент необходимо одномоментно смотреть с другими маркерами холестаза (5-нуклеотидазой, лейцинаминопептидазой или гамма-глютамилтранспептидазой). Уровни данных энзимов обычно повышаются параллельно с повышением уровня щелочной фосфатазы у пациентов с заболеваниями печени, но не повышены при патологии костей.
Следует отметить, что физиологическое повышение щелочной фосфатазы отмечается во время интенсивного роста (например, на первом году жизни, у подростков), у женщин в третьем триместре беременности (из-за притока плацентарной щелочной фосфатазы в кровь).
Низкий уровень ЩФ в сыворотке крови отмечается при гипотиреозе, пернициозной анемии, дефиците цинка, врожденной гипофосфатазии.
Гамма-глутамилтранспептидаза
Референтные значения γ-глутамилтранспептидазы: у детей до 1 месяца – до 163, до года – ниже 91, у женщин – 11–32, у мужчин – 18–50 МЕ.
Гамма-глутамилтранспептидаза (гаммаглутамилтрансфераза, ГГТ) катализирует перенос гамма-глутамилового остатка с гамма-глутамилового пептида на аминокислоту, другой пептид или иной субстрат. В организме человека фермент участвует в метаболизме глутатиона – пептида, состоящего из остатков глутаминовой кислоты, цистеина, глицина, который играет важную роль во многих обменных процессах [7].
Наиболее высокая активность ГГТ обнаружена в почках: в 7000 раз выше, чем в сыворотке крови. Содержание ГГТ в сыворотке крови здорового человека обычно незначительно и связано с ее экскрецией из клеток печени, где активность фермента в 200–500 раз выше. Кроме того, ГГТ содержится в клетках поджелудочной железы (в 600 раз выше, чем в сыворотке крови). Незначительная активность фермента регистрируется в кишечнике, головном мозге, сердце, селезенке, простате и скелетных мышцах. В связи с высоким содержанием ГГТ в тканях простаты, активность ГГТ у мужчин примерно на 50% выше, чем у женщин. В клетке ГГТ локализована в мембране, лизосомах и цитоплазме, причем мембранная локализация фермента характерна для клеток с высокой секреторной, экскреторной или (ре-)абсорбционной способностью.
Несмотря на то, что активность фермента наиболее высока в почках, источник сывороточной активности ГГТ – преимущественно гепатобилиарная система. Данный фермент более чувствителен к нарушениям в клетках печени, чем щелочная фосфатаза.
Как правило, при острых гепатитах активность ГГТ повышается раньше, чем активность АСТ и АЛТ. На пике заболевания активность ГГТ ниже (повышена в 2–5 раз), чем активность аминотрансфераз, и нормализуется значительно медленнее. Это позволяет использовать ГГТ для контроля за выздоровлением больного. Наиболее высокую активность ГГТ (в 5–30 раз выше референтного интервала) наблюдают при внутри- и внепеченочном холестазе. Несколько меньшие значения активности фермента регистрируют при первичных опухолях печени. При злокачественных опухолях другой локализации постепенное увеличение активности ГГТ указывает на наличие метастазов в печени. Активность ГГТ может быть использована в качестве маркера рака поджелудочной и предстательной железы, так как отражает ремиссию и рецидивы заболевания [6].
В связи с тем, что ГГT, помимо клеточной мембраны, содержится в микросомах гепатоцитов, лекарственные препараты из группы индукторов микросомального окисления способны стимулировать ее активность. К индукторам микросомальных ферментов печени относятся снотворные средства (барбитураты, хлоралгидрат), транквилизаторы (диазепам, хлордиазепоксид, мепробамат), нейролептики (хлорпромазин, трифлуоперазин), противосудорожные (фенитоин), противовоспалительные (диклофенак, парацетомол), некоторые антибиотики, гормональные препараты. Поэтому определение активности ГГТ используют для установления гепатотоксичности – она повышается в 90% случаев [6].
В большинстве случаев у таких больных в крови одновременно повышается и активность трансаминаз. Особенно чувствительна активность ГГТ к влиянию на печень длительного потребления алкоголя. У лиц, злоупотребляющих алкоголем, активность ГГТ в сыворотке крови коррелирует с количеством принимаемого алкоголя. Тест особенно ценен для контроля лечения алкоголизма. Прекращение приема алкоголя снижает активность фермента приблизительно на 50% в течение 10 дней.
Уровень ГГТ может увеличиваться в 5–15 раз и при острых и хронических панкреатитах, а также в случаях злокачественных заболеваний поджелудочной железы. Наиболее значимые патологические состояния, вызывающие повышение ее активности, приведены ниже:
- обтурация внутрипеченочных и внепеченочных желчных протоков;
- заболевания печени (острые и хронические гепатиты, лекарственные поражения печени, цирроз печени, опухоли и метастазы в печень);
- панкреатиты и опухоли поджелудочной железы;
- интоксикация этанолом (даже при умеренном употреблении алкоголя).
Лейцинаминопептидаза
Лейцинаминопептидаза (ЛАП) – это протеолитический фермент, гидролизирующий тканевые аминокислоты от N-терминальных белков и полипептидов. Этот фермент обнаружен во всех тканях человека. Самые высокие концентрации фермента выявляются в печени (в основном в желчном эпителии), почках, тонкой кишке.
Сывороточную активность ЛАП в клинической практике определяют в основном для подтверждения синдрома холестаза. ЛАП имеет примерно такое же клиническое значение, как и щелочная фосфатаза. Однако активность ЛАП при заболеваниях костной ткани практически не меняется. Поэтому определение ЛАП используется для дифференциальной диагностики заболеваний гепатобилиарной системы и костной ткани, когда повышена активность щелочной фосфатазы. ЛАП повышается при механической желтухе, при метастазах в печень, даже в отсутствии желтухи, тогда как при других заболеваниях печени, например, при гепатите и циррозе, ее активность повышается в значительно меньшей степени.
Активность ЛАП также может повышаться при острых панкреатитах и холециститах, у больных саркоидозом, системной красной волчанкой, инфекционным мононуклеозом, при опухолях различной локализации. Активность ЛАП возрастает на поздних стадиях беременности, что связано с появлением плацентарной формы фермента в сыворотке крови [6].
5-нуклеотидаза (5-НТ)
5-нуклеотидаза (5-НТ) – фермент, катализирующий гидролиз нуклеотид-5-фосфатов. Фермент распространен во многих тканях организма (печень, мозг, мышцы, почки, легкие, щитовидная железа, аорта). В печени фермент присутствует в желчных канальцах, синусах и клетках Купфера. Повышение активности 5-нуклеотидазы происходит параллельно активности щелочной фосфатазы при холестазах любой локализации, но данный фермент более чувствителен к первичному и вторичному билиарному циррозу, а также к хроническому активному гепатиту [6].
Главное отличие 5-нуклеотидазы от щелочной фосфатазы – отсутствие активности при патологии костной системы.
Желчные кислоты
Желчные кислоты (ЖК) являются надежным маркером холестаза любой этиологии (гепатиты вирусного и токсического генеза, билиарный цирроз, первичный склерозирующий холангит, длительная подпеченочная механическая желтуха, поражение печени при алкоголизме, гепатоцеллюлярная карцинома, острый холецистит, муковисцидоз и др.). Прием некоторых групп лекарственных препаратов может влиять на концентрацию желчных кислот в крови.
Так, повышают результат теста циклоспорин, изониазид, метотрексат, рифампицин, фузидиновая кислота понижает холестирамин. При болезнях печени нарушается удаление желчных кислот из крови воротной вены, что обусловлено как поражением паренхимы, так и портокавальными шунтами. Кроме того, желчные кислоты поступают обратно в кровь из поврежденных гепатоцитов или из желчных путей при их обструкции.
С накоплением в тканях токсичных желчных кислот в настоящее время связывают развитие кожного зуда при синдроме холестаза. Выраженность его может быть разной: от эпизодического, не замечаемого пациентом, до тяжелого, инвалидизирующего (например, при первичном билиарном циррозе).
На генетические дефекты синтеза ЖК приходится приблизительно 1–2% холестатических заболеваний (например, прогрессирующий семейный внутрипеченочный холестаз или болезнь Байлера, дефект амидирования желчных кислот, врожденное нарушение синтеза первичных желчных кислот др.) [8].
Прогрессирующий семейный внутрипеченочный холестаз (в англоязычной литературе – Progressive Familial Intrahepatic Cholestasis – PFIC, ПСВХ) представляет собой группу аутосомно-рецессивных заболеваний, которые манифестируют у новорожденных либо в раннем детском возрасте и приводят к формированию цирроза печени в течение, как правило, первого десятилетия жизни (табл. 2).
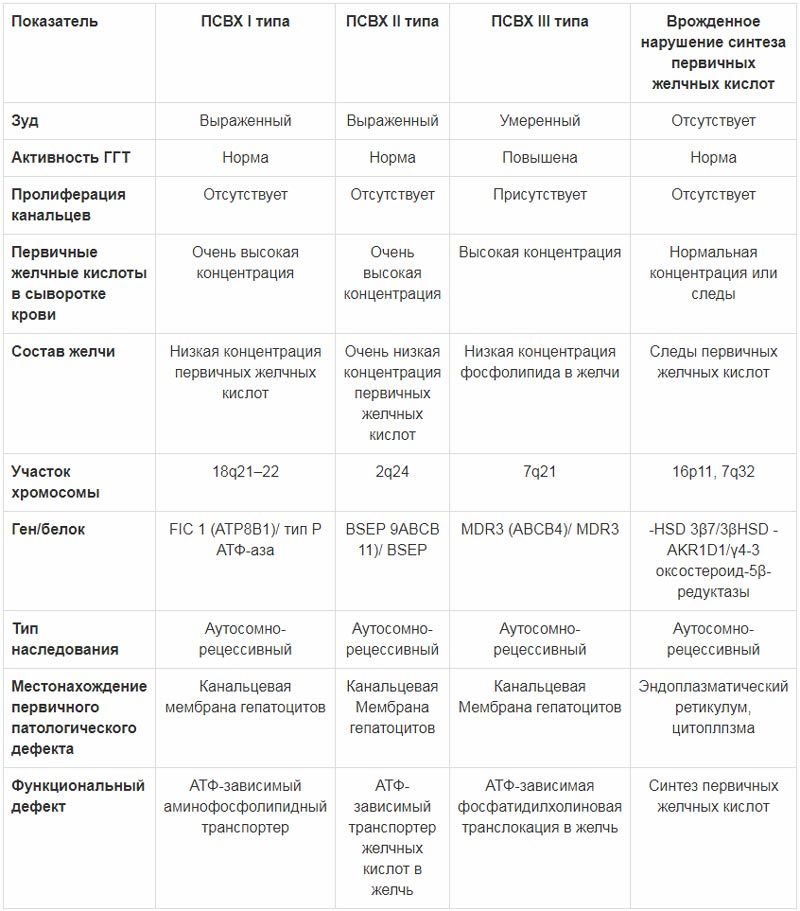
Таблица 2. Основные характеристики прогрессирующего семейного внутрипеченочного холестаза и врожденного нарушения синтеза желчных кислот (А.В. Дегтярева, 2016)
В табл. 3 приведены биохимические показатели при разных формах холестаза [5].
Таблица 3. Лабораторные показатели разных форм холестаза.
| Форма холестаза | Показатели лабораторных тестов |
| Холестаз без желтухи | ЩФ ↑, ЛАП ↑, ГГТ ↑ |
| Холестаз без желтухи, но с повреждением гепатоцитов | ЩФ ↑, ЛАП ↑, ГГТ ↑, АЛТ ↑, АСТ ↑, ГлДГ ↑ |
| Холестаз с желтухой | ЩФ ↑, ГГТ ↑, билирубин ↑, ХС↑ |
| Холестаз с желтухой и повреждением гепатоцитов | ЩФ ↑, ГГТП ↑, билирубин ↑, ХС↑ АЛТ ↑, АСТ ↑, ГлДГ ↑ |
Примечание: ЩФ – щелочная фосфатаза, ЛАП – лейтиаминопептидаза, ГГТ – гамма-глютмилтранспептидаза, АЛТ – аланинаминотрансфераза, АСТ – аспартатаминотрансфераза, ГлДГ – глутаматдегидрогеназа.
При некоторых холестатических заболеваниях печени, обусловленных дефектом синтеза желчных кислот, уровень ГГТ в сыворотке крови может быть низким или в пределах референтных значений (например, врожденное нарушение синтеза первичных желчных кислот).
К дополнительным маркерам холестаза относятся билирубин, холестерин, фосфолипиды и β-липопротеиды. Однако эти показатели могут рассматриваться как маркеры холестаза только при их одновременном повышении с другими биохимическими показателями (ЩФ, ГГТ, 5-НТ, ЛАП).
При выраженном холестазе уровень холестерина может повышаться до 2–4 норм и выше. В свою очередь изолированное повышение холестерина имеет другие причины и не свидетельствует о наличии холестаза у пациента. Учитывая тот факт, что холестерин синтезируется в печени, в случае тяжелой печеночноклеточной недостаточности даже выраженный холестаз может не сопровождаться повышением холестерина (чаще отмечается его снижение в рамках гепатодепрессивного синдрома).
Билирубин в сыворотке крови
Референтные значения концентрации общего билирубина в сыворотке крови у новорожденных детей на первые сутки жизни – до 68 мкмоль/л, у взрослых – 3,4–20,5 мкмоль/л.
Исследование уровня общего билирубина и его фракций проводят для дифференциальной диагностики желтух. В зависимости от того, какой тип билирубина присутствует в сыворотке крови – неконъюгированный (непрямой) или конъюгированный (прямой), гипербилирубинемию классифицируют как неконъюгированную и конъюгированную, соответственно.
Гипербилирубинемия характерна для многих наследственных заболеваний обмена веществ (дефицит α1-антитрипсина, галактоземия, тирозинемия, болезнь Байлера, пероксисомные заболевания, болезнь Ниманна–Пика и др.).
Прямой билирубин в сыворотке крови
Референтные значения содержания прямого билирубина в сыворотке крови – 0–0,2 мг/дл или 0–3,4 мкмоль/л.
При паренхиматозной желтухе наступает деструкция печеночных клеток, нарушается экскреция прямого билирубина в желчные капилляры, и он попадает непосредственно в кровь, где содержание его значительно увеличивается. Кроме того, снижается способность печеночных клеток синтезировать глюкурониды билирубина, вследствие чего количество непрямого билирубина в крови также увеличивается [5].
При механической желтухе нарушено выделение желчи, что приводит к резкому увеличению содержания прямого билирубина в крови. Несколько повышается в крови и концентрация непрямого билирубина. При гемолитической желтухе содержание прямого билирубина в крови не изменяется.
Преимущественно прямая гипербилирубинемия.
- Нарушение экскреции билирубина в желчь.
А. Наследственные нарушения.- Синдром Дабина–Джонсона.
- Синдром Ротора.
- Доброкачественный рецидивирующий внутрипеченочный холестаз.
Б. Приобретенные нарушения.
- Поражение паренхимы печени (например, при вирусном или лекарственном гепатите, циррозе печени).
- Прием некоторых препаратов (пероральные контрацептивы, андрогены, хлорпромазин).
- Алкогольное поражение печени.
- Сепсис.
- Послеоперационный период.
- Парентеральное питание.
- Холестаз беременных.
- Патология желчных протоков.
- Пороки развития желчных путей (стриктуры, атрезия, кисты желчных протоков).
- Билиарный цирроз печени (первичный или вторичный).
- Первичный склерозирующий холангит.
- Болезнь Кароли (врожденное расширение желчных протоков).
- Холедохолитиаз.
- Злокачественные новообразования (холангиокарцинома, рак фатерова соска).
- Гельминтозы (печеночные трематодозы, аскаридоз).
Б. Сдавление.
- Злокачественные новообразования (рак поджелудочной железы, лимфомы, метастазы в лимфатические узлы ворот печени).
- Воспаление (панкреатит).
Непрямой билирубин в сыворотке крови
Исследование непрямого билирубина (НБ) играет важнейшую роль в диагностике гемолитических анемий. Повышение концентрации НБ при гемолитической анемии обусловлено интенсивным его образованием вследствие гемолиза эритроцитов, и печень оказывается неспособной к образованию столь большого количества глюкуронидов билирубина. Содержание непрямого билирубина повышается при желтухе новорожденных, синдромах Жильбера, Криглера–Найяра. При перечисленных синдромах нарушена конъюгация непрямого билирубина с глюкуроновой кислотой.
Преимущественно непрямая гипербилирубинемия.
- Повышенное образование билирубина.
- Гемолиз.
- Неэффективный эритропоэз.
- Талассемия.
- Сниженный захват билирубина в печени.
- Длительное голодание.
- Сепсис.
- Конкурентная связь белков с лекарствами.
- Нарушение коньюгации билирубина.
А. Наследственная недостаточность глюкуронилтрансферазы.- Синдром Жильбера.
- Синдром Криглера–Найяра I типа.
- Синдром Криглера–Найяра II типа.
Б. Физиологическая желтуха новорожденных.
В. Приобретенная недостаточность глюкуронилтрансферазы.- Прием некоторых препаратов (например, хлорамфеникола).
- Желтуха, связанная с грудным вскармливанием.
- Гипотиреоз.
- Поражение паренхимы печени (гепатиты, цирроз).
У пациентов с холестазом и гепатобилиарными заболеваниями глюкораниды билирубина способны прочно связываться с альбумином в сыворотке крови. Таким образом, период полураспада этой фракции билирубина вместо 4-часового распада становится равен полураспаду альбумина (14–20 дней)! Это не связано с состоянием печени.
Гепатопротекторные препараты, применяемые при синдроме холестаза, представлены в табл. 4 [10].
Таблица 4. Эффективность гепатопротекторов при синдроме холестаза (по С. В. Морозову с соавт., 2011 и Н. Б. Губергриц, 2012)
| Препарат | Синдром цитолиза |
| Липоевая кислота | – |
| ЭФЛ | – |
| Препараты животного происхождения | – |
| Силимарин | – |
| L-орнитин L-аспартат | – |
| Адеметионин | + |
| УДХК (Урсодезоксихолевая кислота) | + |
Примечание: (+) – положительный терапевтический эффект; (-) – эффект отсутствует.
Механизмы действия гепатопротекторных препаратов при синдроме холестаза
Адеметионин эффективен при внутридольковом варианте холестаза (нарушение синтеза и тока желчи). Антихолестатический эффект обусловлен повышением подвижности и поляризации мембран гепатоцитов вследствие стимуляции синтеза в них фосфатидилхолина. Это улучшает функцию ассоциированных с мембранами гепатоцитов транспортных систем желчных кислот (ЖК) и способствует пассажу ЖК в желчевыводящую систему. Стимулирует детоксикацию ЖК – повышает содержание в гепатоцитах конъюгированных и сульфатированных ЖК. Конъюгация с таурином повышает растворимость ЖК и выведение их из гепатоцита.
Сульфатирование обеспечивает возможность элиминации ЖК почками, облегчает их прохождение через мембрану гепатоцита и выведение с желчью. Кроме того, сульфатированные ЖК защищают мембраны клеток печени от токсического действия несульфатированных ЖК (в высоких концентрациях присутствуют в гепатоцитах при внутрипеченочном холестазе).
У пациентов с диффузными заболеваниями печени (цирроз, гепатит) с синдромом внутрипеченочного холестаза адеметионин понижает выраженность кожного зуда, улучшает биохимические показатели (уровень прямого билирубина, активность ЩФ, аминотрансфераз и др). Разрешен при внутрипеченочном холестазе беременных в III триместре [2; 11; 12].
Побочные действия: гастралгия; диспепсия; изжога; бессонница, аллергические реакции.
Противопоказания: повышенная чувствительность к компонентам препарата; генетические нарушения, влияющие на метиониновый цикл и/или вызывающие гомоцистинурию и/или гипергомоцистеинемию (дефицит цистатионин бета-синтазы, нарушение метаболизма витамина В12); 1-й и 2-й триместры беременности; период лактации (грудного вскармливания); возраст до 18 лет из-за отсутствия исследований по эффективности и безопасности.
В случае клинической необходимости назначения адеметионина в детской практике вопрос решается через консилиум или при разрешении локального этического комитета при информированном согласии родителей. Наши клинические наблюдения за детьми показали положительный эффект от применения адеметионина в виде снижения ЩФ, ГГТ, нормализации АЛТ и АСТ. Ни у одного из наблюдаемых нами пациентов не было отмечено каких-либо побочных эффектов. Детям до 10 кг назначается 50–100 мг/сут, от 10 до 20 кг 100– 200 мг/сут, выше 20 кг – 200–400 мг/сут [13].
Урсодезоксихолевая кислота (УДХК) – нетоксичная, третичная, гидрофильная желчная кислота, которая стимулирует билиарную секрецию ЖК и других органических анионов (например, глюкоронидов билирубина, конъюгатов глутатиона) и предотвращает индуцированный гидрофобными ЖК холестаз.
УДХК стимулирует экспрессию транспортных белков, необходимых для билиарной секреции в гепатоците, а также продвижение и включение транспортных молекул в каналикулярную мембрану. На фоне приема препарата уменьшается энтерогепатическая циркуляция гидрофобных желчных кислот, предупреждается их токсический эффект на мембраны гепатоцитов и эпителий желчных протоков [2; 14; 15].
Побочные действия: неоформленный стул; аллергические реакции; при лечении первичного билиарного цирроза очень редко – острые боли в правой верхней части живота. При лечении развитых стадий первичного билиарного цирроза очень редко – декомпенсация цирроза печени, которая исчезает после отмены препарата.
Противопоказания: повышенная чувствительность к компонентам препарата; рентгеноположительные (с высоким содержанием кальция) желчные камни; нефункционирующий желчный пузырь; острые воспалительные заболевания желчного пузыря, желчных протоков и кишечника; цирроз печени в стадии декомпенсации; выраженные нарушения функции почек, печени, поджелудочной железы.
Важно отметить, что согласно рекомендациям EASL и РГА УДХК является препаратом выбора при практически любых заболеваниях, протекающих с синдромом холестаза (табл. 5) [2].
Таблица 5. Рекомендации Российской гастроэнтерологической ассоциации по применению УДХК при холестазах (по В. Т. Ивашкину с соавт., 2015)
| Патологическое состояние | Рекомендации |
| Первичный билиарный цирроз (ПБЦ) | УДХК 13–15 мг/кг При «субоптимальном ответе» на прецирротической стадии – УДХК + Будесонид 6–9 мг/сут |
| Первичный склерозирующий холангит (ПСХ) | УДХК (15–20 мг/кг) улучшает печеночные пробы и суррогатные прогностические маркеры, но не об-ладает доказанным влиянием на выживаемость, УДХК может быть рекомендована в группах высокого риска по развитию колоректального рака |
| Перекрестные синдромы (ПБЦ-АИГ, ПСХ-АИГ) | Комбинированная терапия: УДХК и глюкокортикостероиды или другие иммуносупрессанты |
| Муковисцидоз | УДХК (20–30 мг/кг/день) улучшает печеночные пробы и гистологическую картину |
| Другие генетические холестатические заболевания печени | В ряде случаев возможно применение УДХК |
| Лекарственный холестаз | Применение УДХК, адеметионина и кортикостероидов для терапии может быть успешно |
| Холестаз во время беременности (в том числе ВХБ) | При холестатических заболеваниях разрешается применение УДХК во втором и третьем триместрах беременности |
Для ускорения нормализации лабораторных показателей и уменьшения клинических проявлений холестаза целесообразно комбинированное лечение адеметионином (предпочтительно в парентеральной форме) с УДХК.
Все больные с холестазом должны принимать препараты кальция и витамин D перорально в качестве составной части программы по предупреждению остеопороза. В случаях выраженного холестаза при наличии стеатореи или доказанном низком уровне жирорастворимых витаминов следует назначить витамины А, Е и К per os [2].
Жировая болезнь печени – причины, симптомы, лечение и профилактика

Печень – самый крупный и важный орган брюшной полости. Обеспечивает белковый, углеводный и жировой обмен.
Жировая болезнь печени сегодня – очень распространенный недуг. Стереотип о том, что от ожирения печени страдают только люди с избыточным весом и алкоголики, вводит в заблуждение. Это заболевание вызывается не только чрезмерным употреблением алкоголя, но и нездоровым питанием и малоподвижным образом жизни, характерными для значительной части населения.
Средний возраст, в котором обнаруживают жировую дистрофию печени, составляет 50 лет, но в целом частота гепатоза увеличивается с возрастом: от 2,6% детей до 26% лиц в возрасте 40-50 лет.
Что такое жировая болезнь печени?
Здоровая печень должна содержать мало жира или вообще его не содержать. При жировой дистрофии или стеатозе печени жировые капли накапливаются в ее клетках – гепатоцитах.
Стеатоз печени развивается медленно, но даже на ранних стадиях может оказывать негативное влияние на сердечно-сосудистую систему. Также печень не способна достаточно эффективно очищать организм от лишнего холестерина и токсинов.
По мере того как количество поврежденных клеток возрастает до критического уровня, печень уже не в состоянии функционировать.
Жирная печень сама по себе не является большой проблемой. Но жировая ткань – это не инертное образование, она выделяет гормоны и способствует воспалению. Так что у некоторых людей — в среднем у 20% — развивается воспаление жировой печени или стеатогепатит, и это уже нехорошо.
У некоторых стеатогепатит прогрессирует и со временем вместо печеночных клеток развивается соединительная ткань и фиброз – путь к циррозу печени и развитию необратимых изменений в этом органе. Ткань печени замещается соединительной тканью и больше не функционирует. Следовательно, печень плохо выполняет свою работу – не производит, не обезвреживает, не очищает и не метаболизирует. Риск рака печени также выше.
Жировая дистрофия печени — серьезный диагноз, требующий наблюдения.
Поэтому очень важно следить за здоровьем печени и своевременно предотвращать причину заболевания, так как печень – единственный орган, способный восстановиться после развития очень тяжелого заболевания.
Печеночное ожирение чаще всего связано с двумя заболеваниями:
- Неалкогольная жировая болезнь печени или НАТАС;
- Алкогольная жировая болезнь печени или АТАС.
Причины возникновения жировой болезни печени
Почти каждому третьему человеку ставят диагноз жировая дистрофия или стеатоз, или жировой гепатоз печени после УЗИ брюшной полости. Больные с этими диагнозами часто не предъявляют жалоб, поэтому жировая дистрофия печени обнаруживается случайно.
Основные причины жировой дистрофии печени известны:
- Злоупотребление алкоголем. Печень расщепляет алкоголь, вырабатывает избыточную энергию, а организм откладывает ее в виде капелек жира.
- Слишком большое количество потребляемых человеком калорий – нездоровое питание, чрезмерное употребление насыщенных жирных кислот, например, сливочного масла и сахара. Особенно плохо так называемое центральное ожирение – в области живота скапливается лишний жир, потому что из кишечника и сальных оболочек в кровь поступает больше жирных кислот. Они попадают в печень и в ней накапливаются капельки жира.
- Один из метаболических синдромов: избыточный вес, диабет 2 типа, высокий уровень холестерина, гипертония или другие симптомы.
- Малоподвижный образ жизни.
- Нарушение функции инсулина. Инсулин — это гормон, способствующий синтезу белков и жиров в печени, он помогает снизить уровень сахара в крови после еды. В отсутствие инсулина неполное окисление промежуточных жиров в организме может привести к развитию сахарного диабета 2 типа.
- Вирусный гепатит В или С. Однако это случается редко.
- Иногда основная причина – регулярный прием лекарств. Около 99% применяемых лекарств метаболизируются непосредственно в печени. Поэтому потенциально любое лекарство может нанести ей вред. Исследования показывают, что антибиотики и нестероидные противовоспалительные препараты, статины, лекарства, используемые для лечения туберкулеза, грибковых заболеваний и психических заболеваний, с большей вероятностью вызывают повреждение печени.
Неалкогольная жировая болезнь печени
Неалкогольная жировая болезнь печени или НАТАС характеризуется избыточным накоплением жира в печени, что чаще всего встречается у пациентов с избыточным весом и диабетом, но также наблюдается у людей с нормальным весом, особенно у тех, кто не питается регулярно или недостаточно и склонны голодать. Худой трезвенник, но с жирной печенью? К сожалению, никто не застрахован от этого диагноза, потому что это болезнь образа жизни!
Алкогольная жировая болезнь печени
Алкоголь – причина жировой дистрофии печени, особенно если он употребляется регулярно. Однако если прием алкоголя прекратить, то жировая болезнь печени обычно исчезает. В этом существенное различие между алкогольной жировой болезнью печени и неалкогольной жировой болезнью печени.
Способность алкоголя воздействовать на печень во многом определяется дозой вещества. Небольшая доза – не более 10 граммов в день красного вина – даже укрепляет печень. Печень не повреждается и более высокой дозой алкоголя, но она не должна превышать 30 граммов в день. Но некоторые люди очень чувствительны к алкоголю, поэтому у них он может вызвать повреждение печени, даже если они употребляют его очень мало, но каждый день.
Быстрее всего жировая дистрофия печени образуется при регулярном употреблении алкоголя:
1) Для мужчин, если ежедневно выпивается 60 г алкоголя, то есть около 1,5 л пива или 0,6 л вина, или 120 г рома.
2) Для женщин, если ежедневно выпивать 20-40 г алкоголя, то есть примерно 0,5-1,0 л пива или 0,2-0,4 л вина.
Диагностика жировой болезни печени
Печень не болит. Пациенты с ожирением печени обычно не испытывают никаких проблем со здоровьем. Имеются только общие расстройства – слабость, повышенная утомляемость, тяжесть или стеснение в правом верхнем подреберье живота, потому что печень становится больше при отложении жира. Потенциальные проблемы легко диагностировать, поэтому рекомендуется периодически проверять и заботиться о своей печени.
- УЗИ брюшной полости;
- Оценка сопутствующих заболеваний – сахарный диабет, гипертоническая болезнь и другие;
- Анализ крови, обращая особое внимание на ферменты печени – АЛТ, АСТ, ГТФ, следует учитывать и другие показания – глюкозу, холестерин, ЛПНП и ЛПВП.
У пациентов с НАСГ АЛТ часто выше, чем АСТ. Но у больных с АТАС уровень АСТ в крови вдвое превышает уровень АЛТ.
Признаки хронического употребления алкоголя:
- кожные звездочки чаще всего поражают кожу лица;
- массивное расширение сосудов кожи и слизистых оболочек;
- эритема запястья – розовые круглые пятна на коже рук;
- гинекомастия у мужчин – увеличение молочных желез;
- увеличение слюнных желез;
- потливость, тахикардия, тремор рук;
- увеличение объема эритроцитов;
- увеличение ГГТ – фермент, находящийся в печени;
- концентрация АСТ > чем АЛТ.
Лечение
Лечение жировой дистрофии печени основано на устранении ее причин. Если больной употребляет алкоголь, его следует прекратить, а если жировая дистрофия печени обусловлена метаболическим синдромом, то следует контролировать уровень сахара в крови, уровень холестерина и снижать вес.
Основное лечение заключается в уменьшении избыточного жира. Пациентам с НАТАС и ожирением рекомендуется снижение массы тела на 7-10%. Этого можно добиться, сократив потребление калорий, увеличив физическую активность как минимум до двух-трех раз в неделю.
Несколько советов по снижению калорийности пищи:
- количество животных жиров и сахара в рационе должно быть ограничено;
- отказаться от колбас и жирных сортов мяса;
- научиться употреблять несладкий чай или кофе;
- не употреблять молоко и молочные продукты с повышенной или нормальной жирностью;
- ограничить употребление тортов и сладостей;
- не употреблять сладкие напитки;
- не употреблять алкоголь;
- печени понравится средиземноморская диета, основанная на растительных продуктах, рыбе, орехах и оливковом масле.
Если человек не может принять эти меры, то необходим прием лекарств для снижения веса – орлистата или сибутрамина. Если такое лечение не помогает, следует прекратить прием препарата и рассмотреть вопрос об операции по уменьшению жира.
Применение гепатопротекторов – эссенциальные фосфолипиды и силимарин – может способствовать очищению печени и улучшению ее биохимических свойств. Эссенциальные фосфолипиды обладают антиоксидантным и антифибротическим действием. Силимарин – экстракт облепихи. Исследования показали, что силимарин снижает резистентность к инсулину и может привести к снижению и нормализации АСТ и АЛТ.
Профилактика
Здоровая печень любит полноценное питание, и важно, чтобы оно было разнообразным. А именно чтобы клетки печени активно функционировали, им нужны как хорошие ненасыщенные жирные кислоты, так и углеводы для их переработки. Напротив, если человек ест однородную пищу, например, сидит на капустной или рисовой диете, часть клеток печени ленивы. Печень будет «наслаждаться» несколькими чашками кофе в день — доказано, что кофе снижает риск развития фиброза печени.
Чтобы избавиться от жира в печени, не обойтись без регулярных физических нагрузок, желательно с увеличением частоты сердечных сокращений. Подходит как для ходьбы, так и для медленного бега, езды на велосипеде, плавания, гребли, рекомендуются регулярные активные прогулки три-пять раз в неделю не менее получаса.
Даже если вес не уменьшился, жировая масса уменьшится в результате физической активности. Жиры — это триглицериды, которые расщепляются и уходят из печени в мышцы, потому что им нужна энергия для движения. У физически активного человека шансы заболеть стеатогепатитом становятся намного ниже.
Чтобы сохранить здоровье печени, необходимо вести здоровый образ жизни и стараться максимально отказаться и сократить вредные привычки. Своевременная борьба с причинами заболевания – лучшее решение. Профилактика определенно лучше, чем лечение.
Повышенная потливость и странный запах тела после коронавируса: почему возникают, как избавиться
Взрослые пациенты, перенесшие коронавирусную инфекцию COVID-19, часто страдают патологическими проявлениями, которые могут сохраняться от одного месяца до полугода. Это выражается в целом наборе астено-вегетативных реакций. Наряду со слабостью, головокружением, головной болью, депрессивным состоянием, имеется также гипергидроз.
Люди отмечают, что запах пота после коронавируса сильно изменился, усилилась интенсивность выделений. Ниже рассмотрим причины возникновения повышенного потоотделения. Почему пот может неприятно пахнуть, каковы последствия гипергидроза и как справиться с недугом.

Как проявляется постковидная потливость
Избыточная потливость непосредственно в период борьбы с любым вирусом является нормой. При помощи интенсивного потоотделения поддерживается температурный баланс тела. Организм таким способом защищается от перегрева и нарушения различных функций. Одним из неприятных и стойких последствий вирусной атаки является гипергидроз.
В отдельных случаях люди чувствуют потливость по ночам после коронавируса, другие в дневное время. Могут становиться потными голова, ноги, подмышечные впадины, спина, ладони.
Переболевшие кавидом также жалуются, что пот приобрел другой запах. Люди выделяют целый набор «ароматов» – луковый, ацетоновый, бензиновый, и даже «ноты» гари. Это может быть связано как с нарушением обоняния под влиянием вируса, так и с изменением химического состава выделяемого пота.
Онлайн консультация по лечению COVID
Терапевт — 950 рублей
Педиатр — 1 500 рублей
Причины гипергидроза после коронавируса
Причины обильной потливости после коронавируса пока точно неизвестны. Специалисты выделяют несколько факторов, которые могут привести к гипергидрозу. Рассмотрим подробно каждый:
- Прием препаратов. Медики для лечения пациентов с КОВИД-19 используют широкий спектр лекарств – противовирусные, жаропонижающие, антибиотики, гормоны. Возможной причиной гипергидроза может являться изменение гормонального фона из-за приема препаратов. В результате ухудшается работа эндокринной системы.
- Эндокринологические нарушения. На фоне ковида может развиться сахарный диабет, заболевания щитовидной железы. Частым симптомом эндокринных патологий является потливость. Ночные приливы связаны с падением уровня инсулина. При тиреотоксикозе щитовидная железа начинает вырабатывать гормоны в повышенном количестве, что тоже приводит к избыточному потению.
- Поражение ЦНС. Коронавирус способен негативно воздействовать на нервную ткань. Это подтверждается изменением вкусового восприятия и обоняния. Болезнетворное влияние дополнительно оказывают накопившиеся токсины, которые вырабатываются возбудителем.
- Патологии кровеносной системы. Вирус действует непосредственно на свертывающую систему крови, вызывает сгущение, которое приводит к образованию тромбов. Это отражается и на процессах метаболизма. Организм через эпидермис выделяет продукты распада, что сопровождается повышенной потливостью. Такой гипергидроз часто наблюдается ночью и может являться первым предвестником заболеваний сердечно-сосудистой системы.
- Психологические и эмоциональные расстройства. Пандемия коронавируса вызывает у многих людей сильный страх за свое здоровье и близких. В отдельных случаях возникает мощная тревога, которая переходит в панические атаки. Такие состояния часто сопровождаются тахикардией, скачками артериального давления, головокружением, онемением в ногах, повышенным потоотделением. Особенно характерны для тревожного расстройства приливы во время ночного сна.
Чем опасно повышенное потоотделение
Повышенное потоотделение не стоит игнорировать. Такое патологическое проявление может привести к обезвоживанию организма. Если человек отмечает редкое мочеиспускание, ощущает жажду, сухость во рту, заторможенность, тахикардию, то нужно незамедлительно обратиться за врачебной помощью.
Программы реабилитации после коронавирусной инфекции



Консультации: ведущего врача превентивной медицины

Консультации: Смольянинова Е.И.
Что делать при сильной потливости после COVID-19
Методы борьбы с потливостью определяет врач. Но и самостоятельно можно принять меры – например, пересмотреть образ жизни и привычки. Опишем, что ещё необходимо при выявлении проблемы.
К какому специалисту обращаться
Если гипергидроз долго не проходит, пот продолжает пахнуть неприятно, а также ощущается сильная астенизация, необходимо обратиться к терапевту. После осмотра и сбора анамнеза врач может порекомендовать полное обследование, чтобы установить причину проявления.
Специалисты Клиники La Salute разработали программы для восстановления организма и устранения постковидного синдрома. Реабилитация включает исследования и лечение. Оздоровительный курс особенно показан пациентам после искусственной вентиляции легких.
Как убирать потливость
Для скорейшего восстановления организма специалисты рекомендуют пересмотреть питание. Необходимо исключить или ограничить жирную и острую пищу, выпечку. В рацион следует добавить белковые продукты, овощи и фрукты. Дополнительно можно повышать иммунитет с помощью витаминов и минерального комплекса, биодобавок.
Также полезно проводить больше времени на свежем воздухе, совершать пешие прогулки, исключить повышенную физическую нагрузку. Отрегулировать режим сна и бодрствования.
Записаться на тестирование
COVID-19 в Клинике La Salute
Отзывы
КТ показало правостороннюю пневмонию как следствие ковида. После выписки из больницы уже месяц не проходит постоянная слабость, стало потеть тело, часто бросает в жар. Сильное потоотделение появилось еще и ночью в последнее время. Поэтому плохой сон. Пот пахнет луком. Такого противного, тошнотворного запаха раньше никогда не было. От мяса тоже стало тянуть чем-то отвратительным, сероводородом.
Моя тетя после перенесенной короновирусной инфекции боится одна оставаться дома и выходить на улицу, был приступ панической атаки. Сильная фобия опять заболеть. Также испытывает слабость, мучается диареей. Наблюдается резкая потеря веса. По ночам беспокоят сильные приливы жара, все тело стало кидать в пот. Кроме этого изменилось обоняние. Некоторые продукты приобрели ненормальный запах.
После короны сильно потею. Днем стал носить с собой дезодорант. Пот приобрел странный запах, который начал преследовать меня везде. Отдает ужасно гнилью или тухлым. Ночью просыпаюсь от того, что буквально обливаюсь потом с головы до ног. Подушку и постельное белье приходится менять. Спать невозможно. Сильно похудел. Остальные запахи тоже воспринимаются необычно. Я курю, табак пахнет кислым. Мясо есть невозможно, кажется вонючим. Собираюсь избавляться и восстанавливаться от постковидных проявлений и возвращать здоровье.
Перенесла двухстороннюю пневмонию, вызванную вирусом covid. Заболевание протекало тяжело, была направлена в коронавирусный госпиталь. После выписки уже месяц продолжает держаться субфебрильная температура, сохраняется небольшой кашель, воспалился тройничный нерв. Стала уставать. Днем постоянно потеет подмышечная ямка, ладони, шея. Ночью просыпаюсь с мокрой спиной, заливает холодный пот. Запах поменялся, и все воняет чем-то отвратительным. От этих проявлений плохо сплю, наутро чувствую себя разбитой.
Можно ли избавиться от потливости самостоятельно
Если гипергидроз продолжает беспокоить в течение длительного времени после выздоровления, при этом пот неприятно пахнет, по ночам ощущаются сильные приливы, необходимо обратиться за медицинской консультацией и пройти обследование.
В Клинике La Salute специалисты разработали комплексные реабилитационные программы для мужчин и женщин с постковидным синдромом. Врачи помогут восстановить здоровье и силы, избавиться от потливости и других проявлений, возникающих после коронавируса.
Синдром Жильбера
Наследственная доброкачественная дисфункция печени, которая приводит к увеличению в крови уровня свободного билирубина, называется синдромом Жильбера. Многие авторы научных работ не считают эту патологию заболеванием, характеризуя ее как передаваемую наследственным путем конституциональную особенность. В той или иной степени она встречается, как минимум, у 3% населения, а среди жителей Африки ее распространенность достигает 10%. У мужчин синдром Жильбера встречается в несколько раз чаще, чем у женщин, – по разным оценкам, от трех до семи раз.
Общие сведения
Основным внешним признаком синдрома Жильбера служит характерное пожелтение кожных покровов, глазной склеры и слизистых оболочек полости рта. Патология не вызывает структурных изменений в тканях печени и носит периодический характер. Как правило, дефекты обмена до достижения подросткового возраста никак не проявляются и обнаруживаются случайно, при обследовании, проводимом по другой причине.
Врожденная наследуемая патология представляет собой уменьшение выработки в тканях печени фермента глюкуронилтрансферазы, из-за чего в крови остается некоторое количество несвязанного билирубина – продукта распада гемоглобина. Обострение, как правило, происходит из-за:
- вирусной или бактериальной инфекции, протекающей с повышением температуры;
- травмы или хирургической операции;
- у женщин – наступления месячных;
- нарушения рекомендованной диеты, употребления в пищу продуктов, создающих добавочную нагрузку на печень;
- недостаточного питания или голодания;
- чрезмерной инсоляции;
- недостатка сна;
- сильной потери жидкости;
- высоких физических или психологических нагрузок, стрессов;
- приема определенных лекарств, в число которых входят некоторые антибиотики, гормональные препараты, кофеин и др.;
- алкогольной интоксикации.
Различают врожденную форму синдрома Жильбера, причиной которой является дефект гена второй хромосомы, и приобретенную, которая развивается после острого гепатита вирусной этиологии.
В целом, заболевание протекает без серьезных осложнений и с благоприятным прогнозом, хотя и сопровождается понижением детоксикационной функции печени.
Проявления патологии
Латентное течение характерно примерно для трети всех случаев заболевания. Чаще всего патологию обнаруживают в периоде между 13 и 30 годами при обследовании, проводимом по другому поводу – например, во время медицинского освидетельствования молодых мужчин призывного возраста. При обострениях синдрома Жильбера симптомы зависят от формы патологии:
- при диспептической – с тошнотой, изжогой, метеоризмом, металлическим привкусом во рту и болями в правой подреберной области;
- при астеновегетативной – со слабостью, головными болями, повышенным потоотделением, сердцебиениями, нарушениями сна, тревожностью, мышечными болями;
- при желтушной – с ярким желтушным окрашиванием кожных покровов и склер без изменения цвета выделений;
- при латентной – с отсутствием внешних проявлений.
У части пациентов наблюдаются расстройства эмоциональной сферы – депрессивные состояния, раздражительность, беспричинные страхи и приступы паники, а в некоторых случаях повышается склонность к поступкам асоциального характера. Медики объясняют эти расстройства самовнушением, связанным с напряжением психики из-за необходимости посещать врачей, сдавать анализы и проходить обследование.
Точно диагностировать заболевание может только врач. Не откладывайте консультацию — позвоните по телефону +7 (495) 775-73-60
Как определяют заболевание
Наиболее важными методами диагностики синдрома Жильбера являются лабораторные исследования, в числе которых:
- общие анализы крови и мочи – в крови увеличено количество незрелых эритроцитов и слегка пониженный гемоглобин, в моче может присутствовать билирубин;
- биохимический анализ крови – может быть слегка снижен уровень сахара, содержание белков в пределах нормы, АЛТ и АСТ в пределах нормы, отрицательный результат тимоловой пробы;
- анализ крови на билирубин – общее содержание повышено за счет роста непрямого билирубина;
- анализ крови на свертываемость – без отклонений;
- анализ на маркеры вирусных гепатитов – отрицательный.
- возможны анализы на содержание железа в сыворотке и другие пробы, связанные с железом крови.
Кроме того, пациенту в обязательном порядке проводят УЗИ печени, чтобы исключить возможность других печеночных патологий. Размеры печени могут немного увеличиваться в периоды обострений. Молекулярно-генетический анализ венозной крови выполняют редко из-за его высокой стоимости, однако он позволяет определить дефектную ДНК, которая является причиной синдрома Жильбера.
Чтобы подтвердить диагноз, проводят нагрузочные пробы:
- с голоданием – при полном голодании либо при ограничении калорийности уровень свободного билирубина повышается в 2-3 раза;
- с фенобарбиталом – после пятидневного приема уровень свободного билирубина понижается;
- с никотиновой кислотой – внутривенная инъекция препарата повышает уровень свободного билирубина в 2-3 раза;
- с рифампицином – введение препарата приводит к увеличению количества билирубина.
Чтобы исключить хронический гепатит или цирроз, может быть назначена пункция печени.
Как снизить билирубин?
Поскольку патология не приводит к резкому ухудшению состояния пациента, то лечение синдрома Жильбера обычно сводится к формированию образа жизни, при котором риск обострения и повышения уровня билирубина будет сведен к минимуму. Для этого пациент должен избегать:
- чрезмерных физических нагрузок – занятий спортом, тяжелого физического труда;
- голодания и недостатка жидкости;
- длительного пребывания на солнце;
- употребления алкоголя;
- приема препаратов с побочным токсическим воздействием на печень.
Важнейшее значение приобретает специальная диета при синдроме Жильбера, которой необходимо придерживаться в течение всей жизни, но наиболее тщательно в периоды обострений. В питании должны преобладать каши, преимущественно гречневая и овсянка, овощные блюда, обезжиренные или маложирные молочные продукты, нежирные сорта мяса, птицы и рыбы. Желательно исключить из меню сладости, выпечку, шоколад, жирные и острые блюда. Порции должны быть небольшими, интервалы между приемами пищи – уменьшенными.
Во время обострений могут назначаться курсы витамина В6 и пищеварительных ферментов, а также короткие курсы фенобарбитала – вещества, связывающего свободный билирубин.
Часто возникающие вопросы
Чем опасен синдром Жильбера?
Сам по себе синдром Жильбера не создает опасности для здоровья и самочувствия. Однако при повышении уровня свободного билирубина постепенно может понижаться выделение желчи, развиваться желчнокаменная болезнь, холецистит или дуоденит.
Почему при синдроме Жильбера нельзя загорать?
Из-за негативного влияния солнечного ультрафиолета на функцию печени загорать при синдроме Жильбера нежелательно ни на открытом солнце, ни в солярии. Прямого запрета нет, но длительная инсоляция может активизировать увеличение несвязанного билирубина. Поэтому желательно выходить на пляж на короткое время (не более получаса) и делать это только в утренние или вечерние часы.
Как передается синдром Жильбера?
Это генетическая патология с аутосомно-доминантным типом наследования, т.е. при наличии у одного из родителей ребенок получает заболевание в 50% случаев.
Холестерин: нормальный, низкий и высокий — нормы для взрослых и детей

Студент медицинского факультета УЛГУ. Интересы: современные медицинские технологии, открытия в области медицины, перспективы развития медицины в России и за рубежом.
Холестерин — элемент, необходимый для нормальной работы организма. В то же время это одна из основных причин развития сердечно-сосудистых патологий. Так как что же такое холестерин? Нужно ли его бояться и контролировать?
В этой статье мы развеем распространенные мифы о роли холестерина и его метаболизме в организме и рассмотрим наиболее эффективные способы контроля уровня холестерина.
Что такое холестерин?
Холестерин (от греческого chole — желчь и stereo — твердый, твердый) — это природный, нерастворимый в воде липофильный (жирный) спирт. Это сложное вещество, состоящее из жира и группы алкоголя, по своей структуре похожее на желчь (за что и получило свое название), входит в состав каркаса клеток и участвует в синтезе жизненно важных веществ, в том числе гормонов. Около 80% холестерина синтезируется в организме (печень, кишечник, почки, надпочечники, половые железы), остальные 20% должны поступать из пищи.
Распространенное мнение, что холестерин всегда вреден, неверное. Без холестерина невозможна нормальная работа организма. При этом уровень холестерина в крови зависит от таких факторов, как пол и возраст человека.
Холестерин, циркулирующий в кровотоке, при необходимости используется как строительный материал, а также для синтеза более сложных соединений. Входя в состав клеточных мембран, он придает им прочность, обеспечивает обмен веществ между клеточными и неклеточными веществами и регулирует действие ферментов.
Поскольку холестерин не растворяется в воде и крови, его транспортировка возможна только в виде сложных водорастворимых соединений, делящихся на 2 вида липопротеинов:
Большую клиническую роль играет соотношение холестерина, присутствующего в этих контейнерах-носителях. Оба вещества должны находиться в строго определенной пропорции, их общий объем также не должен превышать норму. Это может привести к серьезным заболеваниям сердечно-сосудистой системы.
Высокий уровень холестерина в крови называется гиперхолестеринемией.
Функции холестерина
В норме холестерин не наносит вреда организму, а, наоборот, выполняет множество важных функций:
- Строительная. Жирный спирт — компонент мембраны каждой клетки организма, обеспечивающий прочность клеточных стенок, регулируя их проницаемость для различных молекул. Задействован в формировании новых синапсов (связей) в головном мозге, что влияет на умственные способности и память. Его самая высокая концентрация обнаружена в эритроцитах и нейронах головного мозга.
- Синтез. Участвует в выработке половых гормонов (тестостерона, эстрогена), кортизола, в синтезе витамина D, стероидов (кортизон, гидрокортизон).
- Пищеварительная. Способствует синтезу желчных кислот, необходимых для нормального переваривания пищи и усвоении жиров в пищеварительном процессе;
- Защитная. Под воздействием солнечных лучей влияет на образование витамина D в коже, укрепляет иммунную систему.
Эти функции реализуются при нормальном уровне общего холестерина в крови и правильном балансе между его фракциями. Оптимальное значение его концентрации в плазме крови составляет менее 5,2 ммоль/л. Максимально допустимое значение составляет 5,2-6,2 ммоль/л, а показатель выше 6,2 указывает на наличие патологии и высокий риск развития сердечно-сосудистых патологий.
Чем опасен высокий холестерин?
Ущерб здоровью наносится не холестерином как таковым, а его излишками или недостатком в организме. У людей, погибших от сердечно-сосудистых заболеваний, часто наблюдается низкий уровень липопротеидов высокой плотности с одновременно высоким содержанием липопротеидов низкой плотности.
Липопротеины при неправильном соотношении или длительном повышенном уровне в крови оседают на стенках сосудов, вызывая атеросклероз.
Это опасное заболевание, при котором на эндотелии (внутренний слой) сосуда образуются бляшки. Они со временем растут, в результате просвет сосудов сужается, а стенки сосуда теряют эластичность (стеноз). Процесс приводит к уменьшению поступления кислорода и питательных веществ к сердцу и тканям и развитию стенокардии.
При стенокардии прекращается снабжение артериальной кровью сердца из-за закупорки коронарной артерии. Состояние сопровождается болью в грудной клетке. Результат нарушения кровоснабжения — инфаркт миокарда.
В результате образования холестериновых бляшек повреждаются внутренние стенки сосудов. Может образоваться сгусток, который затем может закупорить артерию и вызвать эмболию — полное перекрытие сосуда. Кроме того, потерявший эластичность сосуд может лопнуть из-за увеличения давления кровотока.
Что такое ЛПВП и ЛПНП — роль липопротеинов высокой и низкой плотности
ЛПВП — хороший липопротеин — альфа-холестерин. Чем выше его процент относительно плохого липопротеина, тем лучше. ЛПВП обладает уникальными антиатерогенными свойствами: он способен растворять холестериновые бляшки и удалять налет со стенок артерий, отправляя плохой холестерин обратно в печень на переработку в желчные кислоты. Поэтому, его повышенная концентрация называется «Синдромом долголетия».
ЛПНП — условно «плохой» холестерин. Образуется в печени из ЛПОНП (липидов очень низкой плотности) при гидролизе. Условно плохим (а не абсолютно) он называется, потому что он также важен для здоровья. Основные его функции — защита организма от токсинов, присутствующих в плазме крови, транспортировка витамина Е, каротиноидов и триглицеридов.
Отрицательное качество липопротеинов низкой плотности, делающее их «плохими» – способность оседать на стенках артерий, образуя жировые пятна. По мере увеличения содержания этого соединения, крупные нерастворимые молекулы сливаются в жировые бляшки и закупоривают сосуды. После окисления холестерин теряет стабильность и может легко проникать в толщу стенок артерий.
Процесс провоцирует выработку специфических антител, что вызывает тяжелое повреждение артерий. Кроме того, такой холестерин способствует снижению уровня оксида азота, повышая риск развития сердечно-сосудистых заболеваний.
Оксид азота (NO) играет важную роль в организме:
- расширяет сосуды, снижает артериальное давление, предотвращает образование тромбов в кровотоке;
- играет важную роль в борьбе с бактериями и вирусами, попавшими в организм, уничтожает раковые клетки;
- повышает выносливость мышечной ткани;
- участвует в обмене информацией между разными клетками, являясь нейромедиатором (передатчик нервного импульса) в синапсах (связи между нейронами).
ЛПВП выводит холестерин из крови обратно в печень и предотвращает окисление ЛПНП.
Симптомы повышенного холестерина в организме
Повышение уровня холестерина связано с нарушением липидного (жирового) обмена. Показатель может быть симптомом атеросклероза и других серьезных заболеваний:
- печени;
- почек — хронической почечной недостаточности, гломерулонефрита;
- поджелудочной железы — хронического панкреатита;
- сахарного диабета, связанного с нарушением работы бета-клеток в островках Лангерганса поджелудочной железы;
- гипотиреоза, при котором снижается синтез гормонов в щитовидной железе;
- ожирения.
Симптомы атеросклероза вызваны сужением просвета сосудистого русла в результате длительного и стойкого высокого уровня холестерина, а также ухудшением кровообращения в разных отделах кровотока.
Основные симптомы патологии:
- стенокардия — внезапный дискомфорт или боль в груди в результате физических упражнений или эмоционального стресса;
- одышка;
- аритмия — проблемы с сердечным ритмом;
- цианоз (посинение) и отек пальцев рук, ног;
- периодические судороги ног;
- ухудшение памяти;
- снижение интеллектуальных способностей;
- желтовато-розовые липидные (жировые) отложения в коже (ксантомы) век и в области голеностопных суставов.
Как проверить уровень холестерина — липидограмма
В целях детальной диагностики и расчета риска возможных осложнений врачи используют расширенный анализ – липидограмму, показывающую общую концентрацию холестерина и его состав. Биохимические анализы крови с определением фракций холестерина часто назначают кардиологи и эндокринологи.
Липидограмма это анализ крови, взятой из вены, показывающий следующие результаты:
- Уровень ЛПНП — количество атерогенного холестерина.
- Уровень ЛПВП — количество хорошего холестерина.
- Количество триглицеридов — основного источника энергии, при распределении которой выделяется 9 ккал.
Показания к анализу липидов:
- стенокардия;
- ишемическая болезнь сердца;
- сахарный диабет;
- патологии щитовидной железы;
- избыточный вес;
- патологии почек, печени.
В Европе анализ на холестерин рекомендуется выполнять каждые 5 лет и по возрасту: 40, 50, 60 лет из-за повышенного риска развития атеросклероза в пожилом возрасте. Также прямые показания для анализа:
Своевременная диагностика повышенного холестерина уберегает от инсульта и преждевременной смерти.
Специальной подготовки анализ не требует, но уровень холестерина определяется натощак, после 8-часового перерыва в еде.
Чтобы получить достоверный результат перед анализом нужно соблюдать ряд правил:
- Диета. За два дня до анализа из меню следует исключить жирную, жареную на масле пищу.
- Вредные привычки. Не пейте алкоголь и не курите перед тестом.
- Лекарства. Предупредите об их приеме врача заранее. Повлиять на результаты исследования могут многие препараты: статины, фибраты, противовоспалительные средства, антибиотики, витамины и БАДы.
Расшифровка анализа на холестерин
Важно понимать, что уровень холестерина в крови у женщин и мужчин, молодых и старых, здоровых и больных – разный. Кроме того, биохимический анализ крови проводится с использованием методов и анализов, которые отличаются в разных лабораториях. Поэтому расшифровку результатов анализа на холестерин проводит лечащий врач.
В результатах анализа можно встретить следующие обозначения:
- КА – коэффициент атерогенности, показывающий отношение ЛПНП к ЛПВП;
- ммоль/л – мера количества миллимолей на литр раствора;
- CHOL – общий холестерин.
Уровень холестерина измеряется в ммоль/л. В редких случаях – мг/дл.
Уровни ЛПВП и ЛПНП
Отклонение уровней липопротеинов ЛПВП и ЛПНП влияет на состояние здоровья, но гораздо важнее соотношение хороших липопротеинов с плохими. Поэтому при определении содержания липопротеинов в крови учитываются 4 показателя:
- общее количество холестерина;
- количество ЛПВП, ЛПНП по отдельности;
- соотношение триглицеридов (коэффициент атерогенности).
Средние нормы общего холестерина в крови у взрослых людей – 3,0 – 5,0 ммоль/л. При угрозе атеросклероза общий уровень холестерина повышается до 7,8 ммоль/л.
Таблица 1. Норма холестерина и триглицеридов у взрослых людей в зависимости от пола
| Пол | Нормы ЛПНП, ммоль/л | Нормы ЛПВП, ммоль/л | Триглицериды, ммоль/л |
| У мужчин | 2,25 – 4,82 | 0,72 – 1,73 | 0,52 – 3,7 |
| У женщин | 1,92 – 4,51 | 0,86 – 2,28 | 0,41 – 2,96 |
Наиболее показательно соотношение ЛПВП и ЛПНП к общему холестерину. У здоровых людей индекс ЛПВП намного выше, чем ЛПНП.
В официальных рекомендациях ESA (Европейское общество по изучению атеросклероза) и HOA (Национальное общество по атеросклерозу) говорится о том, что нормальный уровень холестерина не является статичным показателем: он меняется с годами. Более подробные цифры можно найти в таблице ниже.
Таблица 2. Нормы холестерина в крови у детей, подростков и взрослых в зависимости от возраста
| Возраст | Пол | Общий, ммоль/л | ЛПНП, ммоль/л | ЛПВП, ммоль/л |
| Новорожденные | 1.38 – 3.60 | |||
| От 3 месяцев до 2 лет | 1.81 – 4.53 | |||
| От 2 до 5 лет | мальчик | 2.95 – 5.25 | ||
| девочка | 2.90 – 5.18 | |||
| 5 – 10 лет | мальчик | 3.13 – 5.25 | 1.63 – 3.34 | 0.98 – 1.94 |
| девочка | 2.26 – 5.30 | 1.76 – 3.63 | 0.93 – 1.89 | |
| 10 – 15 лет | мальчик | 3.08 – 5.23 | 1.66 – 3.34 | 0.96 – 1.91 |
| девочка | 3.21 – 5.20 | 1.76 – 3.52 | 0.96 – 1.81 | |
| 15 – 20 лет | юноша | 2.91 – 5.10 | 1.61 – 3.37 | 0.78 – 1.63 |
| девочка | 3.08 – 5.18 | 1.53 – 3.55 | 0.91 – 1.91 | |
| 20 – 25 лет | мужчина | 3.16 – 5.59 | 1.71 – 3.81 | 0.78 – 1.63 |
| женщина | 3.16 – 5.59 | 1.48 – 4.12 | 0.85 – 2.04 | |
| 25 – 30 лет | мужчина | 3.44 – 6.32 | 1.81 – 4.27 | 0.80 – 1.63 |
| женщина | 3.32 – 5.75 | 1.84 – 4.25 | 0.96 – 2.15 | |
| 30 – 35 лет | мужчина | 3.57 – 6.58 | 2.02 – 4.79 | 0.72 – 1.63 |
| женщина | 3.37 – 5.96 | 1.81 – 4.04 | 0.93 – 1.99 | |
| 35 – 40 лет | мужчина | 3.63 – 6.99 | 1.94 – 4.45 | 0.88 – 2.12 |
| женщина | 3.63 – 6.27 | 1.94 – 4.45 | 0.88 – 2.12 | |
| 40 – 45 лет | мужчина | 3.91 – 6.94 | 2.25 – 4.82 | 0.70 – 1.73 |
| женщина | 3.81 – 6.53 | 1.92 – 4.51 | 0.88 – 2.28 | |
| 45 – 50 лет | мужчина | 4.09 – 7.15 | 2.51 – 5.23 | 0.78 – 1.66 |
| женщина | 3.94 – 6.86 | 2.05 – 4.82 | 0.88 – 2.25 | |
| 50 – 55 лет | мужчина | 4.09 – 7.17 | 2.31 – 5.10 | 0.72 – 1.63 |
| женщина | 4.20 – 7.38 | 2.28 – 5.21 | 0.96 – 2.38 | |
| 55 – 60 лет | 4,45 — 7,7 | |||
| 60 – 65 лет | 4,45 — 7,69 | |||
| 65 – 70 лет | 4,43 — 7,85 | |||
| Старше 70 лет | 4,48 — 7,25 |
Холестерин у пожилых мужчин
Как видно из таблицы, уровень холестерина у представителей сильного пола постепенно повышается с возрастом. Так, у мужчин после 40 лет уровень холестерина колеблется в пределах 3,91-6,86 ммоль/л, после 50 лет – от 4,2 до 7,7 ммоль/л, а после 60 лет наблюдается высокий уровень холестерина.
Холестерин у женщин после 40 лет
У женщин уровень холестерина в крови, как правило, стабилен до наступления менопаузы. После наступления климакса уровень холестерина повышается. Статистика говорит о том, что половина женщин в возрасте 50 лет и старше имеют высокий уровень ЛПНП и низкий уровень ЛПВП.
Нормы холестерина у женщин после менопаузы:
- в 40 – 50 лет – 1,92-4,82 ммоль/л;
- в 50 – 60 лет – 2,28-5,44 ммоль/л;
- после 60 лет – 2,6-5,8 ммоль/л.
При значительном превышении допустимого порога нужно изменить меню и начать прием препарата для снижения холестерина.
Нормы холестерина при беременности
Беременные женщины требуют особого внимания, так как в этот период происходит множество изменений, в том числе и уровня холестерина.
Таблица 3. Нормы холестерина у беременных в зависимости от возраста
| Возраст беременной женщины, лет | Референсные значения общего холестерина, ммоль/л |
| 20 – 25 | 6,34-11,2 |
| 25 – 30 | 6,6–12,6 |
| 30 – 35 | 6,8 – 11,94 |
| 35 – 40 | 7,4-12,6 |
Будущим мамам необходимо следить за уровнем холестерина и своевременно его корректировать, так как это вещество влияет на женский организм, течение беременности и на здоровье плода.
Причины плохого результата анализа на холестерин
Результаты липидограммы могут указывать на множество различных аномалий в липидном обмене. Чаще повышение общего холестерина из-за фракции ЛПНП свидетельствует о следующих патологиях:
- врожденная гиперлипидемия;
- заболевания внутренних органов — печени, почек, поджелудочной железы; ;
- гипотиреоз.
Ученые выделили несколько основных факторов, способствующих повышению уровня холестерина в крови:
- Пассивный образ жизни. При недостаточной подвижности повышается уровень «плохого» холестерина, что провоцирует развитие сердечно-сосудистых заболеваний.
- Ожирение. Избыточный вес – тяжелая нагрузка на организм. Даже несколько лишних килограммов поднимают уровень плохого холестерина, поэтому люди с избыточным весом склонны к различным заболеваниям сердечно-сосудистой системы. При этом лишний вес трансформируется в ожирение незаметно. Например, ожирение в пожилом возрасте гарантирует средняя ежегодная прибавка в весе с 20 до 30 лет всего на 2,1 кг.
- Курение. Никотин стимулирует сужение артерий, повышение вязкости крови, тромбоз.
- Диета с большим количеством жирных продуктов.
- Наследственность. Предрасположенность к высокому холестерину передается генетически. Семейная гиперхолестеринемия увеличивает риск ранних сердечных заболеваний. Поэтому люди с отягощенной наследственностью должны регулярно сдавать анализы на холестерин.
- Климакс. Во время менопаузы уровень эстрогена снижается. А это приводит к увеличению ХОЛ и ЛПНП, в том числе триглицеридов и снижению ЛПВП. Такое нездоровое состояние женского организма восстанавливается с помощью гормональной терапии, что порой приводит к негативным последствиям.
- Психологический стресс. Женщины, пережившие нервное потрясение, часто имеют высокий уровень холестерина. Одна из причин — «заедание» стресса сладостями, буквально напичканными насыщенными жирами и плохим холестерином.
Также возможно снижение уровня холестерина. Как правило, низкий холестерин связан со следующими патологиями:
- гипопротеинемией; ; , заболеваниями кроветворной системы; , раком печени;
- хроническими заболеваниями легких.
Низкий уровень холестерина наблюдается у вегетарианцев и голодающих людей. Также часто обнаруживается у пациентов с ожогами, сепсисом.
Источники:
- https://www.fdoctor.ru/health/helpful_information/dieta_i_kholesterin_produkty_kotorye_pomogut_uluchshit_vashi_pokazateli/
- https://medi.ru/pp/arhiv/zhurnal_praktika_pediatra_arhiv_za_2017_god/sentyabr_-_oktyabr_2017/13649/
- https://medcentr-diana-spb.ru/endokrinologiya/zhirovaja-bolezn-pecheni-prichiny-simptomy-lechenie-i-profilaktika/
- https://lasalute-clinic.ru/covid-19/silnaya-potlivost-posle-koronavirusa
- https://www.medicina.ru/patsientam/zabolevanija/sindrom-zhilbera/
- https://unclinic.ru/holesterin-normalnyj-nizkij-i-vysokij-normy-dlja-vzroslyh-i-detej/
